Für Sie kommentiert
Niedrigeres Risiko für Zervixdysplasien bei Kupferspiralenträgerinnen?/ Prä‑ und intraoperative Lidocaininfusionen vermindern postoperative Schmerzen/Vertikale HPV-Übertragung/Mammographiescreening ab 40 Jahren?/Outcome der Schwangerschaft und spätere rheumatologische Erkrankungen
Niedrigeres Risiko für Zervixdysplasien bei Kupferspiralenträgerinnen?
Ein Einfluss auf das Risiko für höhergradige Zervixdysplasien und Zervixkarzinome durch IUD ist immer wieder diskutiert worden. Viele Studien zeigen einen moderaten protektiven Effekt. Eine aktuelle retrospektive Kohortenstudie an einem nordamerikanischen Patientinnenkollektiv mit über 10 000 Patientinnen beschäftigte sich nun mit der Frage, ob die Art des IUD (Levenorgestrel[LNG]-IUD versus Kupfer[CU]-IUD) einen Einfluss auf diesen Effekt hat. Etwa drei Viertel der Patientinnen, deren medianes Alter bei 29 Jahren lag, hatten ein Cu-IUD erhalten. Die Follow-Up-Zeit betrug für beide Kohorten etwa neun Jahre im Median, bei 22 % (Cu) respektive 33 % (LNG) erfolgte im Laufe dieser Zeit die Entfernung des IUD. Bei der Analyse erfolgte die Adjustierung auf einige demographische und anamnestische Variablen. Im Verlauf wurde bei 0,7 % der Cu-IUD-Trägerinnen und bei 1,8 % der LNG-IUD-Trägerinnen eine high-grade zervikale Neoplasie diagnostiziert, die relative Risikoreduktion lag bei 0.38. Die Autoren folgern, dass ein Cu-IUD im Vergleich zum LNG-IUD einen protektiven Effekt hat (Spotnitz M. E. et al., Obst & Gynecol 2020; 135,2:319–27)
Kommentar
Eine interessante Studie, leider mit einigen Schwächen. Die grösste ist sicher das Fehlen eines Vergleichskollektivs mit Nicht-IUD-Trägerinnen. Es muss auch bedacht werden, dass die Indikationsstellung für LNG-IUD weiter gefasst ist, namentlich für Blutungsstörungen, und die Kohorten daher eine gewisse Dysbalance haben könnten. Die Gesamtinzidenz von Neoplasien ist gering. Denkbar ist ein Effekt allerdings: Kupferionen könnten einen positiven Effekt auf die Ausheilung von HPV-Infektionen haben, ob LNG dagegen einen permissiven Effekt hat, ist umstritten.
Martin Heubner
Prä- und intraoperative Lidocaininfusionen vermindern Schmerzen nach laparoskopischen Operationen
In einer methodisch sauberen, prospektiv randomisierten Doppelblindstudie bei Patientinnen, die sich einer laparoskopischen Inguinalhernien-OP unterzogen, erhielt die Therapiegruppe Lidocain 2 % (zuerst einen Bolus 1.5 mg/kg gefolgt von einer Infusion mit 2 mg/kg/Stunde) zu Beginn der Anästhesieeinleitung bis hin zur Extubation.
Der primäre Outcome Parameter war der Morphiumverbrauch innert der ersten 24 Stunden; sekundär wurden postoperative Schmerzscores, Übelkeit/Erbrechen (PONV) sowie die Qualität der Erholung (QoR-40 Scores) untersucht.
Die Vergleichsgruppe erhielt das gleiche Volumen als NaCl-Lösung.
Resultate
Der Morphiumverbrauch innert 24 Stunden war (0–1)mg in der Lidocaingruppe vs. 4 mg in der Kontrollgruppe (p<0,001). Die postoperativen Schmerzscores waren ebenfalls signifikant niedriger (p<0.05), ebenso PONV (p<0.05).
Die medianen QoR-Scores nach 24 Stunden waren signifikant besser :194(194–196) als in der Placebogruppe:188(183–186), p<0.02.
Die Patientenzufriedenheit war signifikant höher (p = 0.02) in der Therapiegruppe (Ghimire, A et al., BMC Anesthesiology 2020; 20:137)
Kommentar
Auch bei minimalinvasiven Operationen hat das Schmerzmanagement noch Verbesserungspotenzial. Im Rahmen der „fast-track“-Chirurgie reduziert man das Auftreten akuter postoperativer Schmerzen durch eine präventive Analgesie (z. B. 1 g Paracetamol 20 min vor OP Ende i.v.) (erfahrungsgemäss wird dies aber oft nicht gemacht).
Mit dem obigen Lidocaine-Regime, das bereits präoperativ beginnt, geht man in die gleiche Richtung, aber mit einer relativ niedrigen und dementsprechend unbedenklichen Dosierung.
Da Lidocain mehrere Schmerzwege beeinflusst, ist es ein interessanter Spieler in einem multimodalen Schmerzpräventionskonzept.
Auch in einer kürzlich veröffentlichten Cochrane Studie zeigte sich eine signifikante Verminderung des postoperativen Opiatverbrauchs unter Lidocain (Weibel, S et al., Cochrane Database Syst. Rev.2018;6:CD009642).
Die Frage ist noch unbeantwortet, ob ein Weiterführen der Lidocaininfusion nach Aufwachen der Patientinnen eine weitere Verbesserung bringt.
Bemerkenswert ist auch die Reduktion von PONV (Übelkeit/Erbrechen), wahrscheinlich, weil unter Lidocain weniger Opioide gegeben wurden.
Zusammengefasst ein interessanter, einfacher Ansatz, um die postoperative Phase weiter zu verbessern.
Michael K. Hohl
Vertikale HPV-Übertragung
Bei Kindern kann das humane Papillomavirus (HPV) eine rezidivierende, respiratorische Papillomatose (RRP) verursachen, eine benigne und sehr seltene Krankheit, welche fast immer durch Low-risk-HPV-Subtypen (v. a. 6 oder 11) induziert wird [1]. Maligne Tumoren im Mund- und Halsbereich sind in etwa 25 % ebenfalls mit HPV assoziiert, v. a. mit den onkogenen Subtypen, welche auch in den Zervixdysplasien und -karzinomen oder anogenital gefunden werden [1, 2]. HPV ist zweifelsohne eine sexuell übertragene Krankheit. Im Falle der HNO-Tumoren ist dies meist bedingt durch oralen Sex oder durch Selbstinokulation [3, 4]. Somit sind auch nicht-sexuelle Wege der Übertragung möglich.
Eine vertikale Transmission von der infizierten Mutter auf das Kind wurde mehrfach beschrieben, wobei die Sectio in früheren Studien eher protektiver zu sein scheint als die vaginale Geburt [5, 6]. Die primäre Sectio schliesst aber eine perinatale Übertagung nicht aus [7, 8]. Eine horizontale Übertragung von HPV beim Stillen ist ebenfalls möglich, wird aber sehr kontrovers diskutiert [9]. So wurde interessanterweise keine Korrelation gefunden zwischen den in der Muttermilch und der oralen Mucosa der Säuglinge nachgewiesenen HPV-Subtypen, wohl aber mit denjenigen der Mundmucosa des Partners! [10]
Es gibt kaum saubere, prospektive Studien mit vergleichbaren Einschlusskriterien und Labormethoden zur HPV-Detektion und -Typisierung. Entsprechend sind die verschiedenen Metaanalysen durch eine mehr oder weniger ausgeprägte Heterogenität geprägt und müssen entsprechend mit Vorsicht interpretiert werden. In der Literatur wird von Transmissionsraten zwischen 2.8 und 39.7 % berichtet [11, 12]. In einer der letzten Metaanalysen, welche ich gefunden habe, lag die vertikale Transmissionsrate bei 4.9 % (95 % CI 1.651–9.849) und die Sectio schien hier nicht mit einer geringeren Transmissionsrate assoziiert zu sein (pooled RR = 0.912, 95 % CI 0.226–3.674, I2 = 24.48 %) [6]. Insgesamt scheint die vertikale Transmissionsrate doch geringer auszufallen, als man erwartet hat.
Spannend wird es sein zu verfolgen, wie sich diese Transmissionsrate im Zeitalter der HPV-Impfung verhalten wird. Bekanntlich verursacht diese Impfung eine stärkere Antikörperreaktion als eine genuine HPV-Infektion. Ein Vergleich der HPV-IgG zwischen Mutter und Neugeborenem konnte zeigen, dass eine hohe Korrelation besteht für die Subtypen 6, 11, 16 und 18 [13]. Das spricht nicht unbedingt für eine vertikale HPV-Transmission, sondern für den physiologischen, transplazentaren IgG-Transfer zwischen Mutter und Kind. Die Antikörper verschwinden innerhalb von 12–24 Monaten nach der Geburt praktisch vollständig [12]. Wahrscheinlich könnten diese Antikörper auch protektiv wirken auf die horizontale HPV-Transmission bei der Geburt oder gar beim Stillen? Entsprechende Studien bei Frauen nach HPV-Impfung fehlen zurzeit gänzlich.
Literatur
1. Tumban
E., Viruses 2019; 11:922.
2. Syrjänen
S., APMIS 2010; 118: 494–509.
3. Sonnex
C et al., Sex Transm Infect 1999; 75:317–9.
4. Winer
RL, et al., Cancer Epidemiol Biomarkers Prev 2010; 19: 1682–5.
5. Medeiros
LR et al., Cad Saude Publica 2005; 21:1006–15.
6. Zouridis
A et al., Archives of Gynecology and Obstetrics 2018; 298:35–44.
7. Chatzistamatiou
K, et al., J Obstet Gynaecol 2016; 36:10–4.
8. Tseng
CJ, et al., Obstet Gynecol 1998; 91: 92–6.
9. Yoshida
K et al., J Obstet Gynaecol 2011; 31:503–6.
10. Louvanto
K et al., Pediatr Infect Dis J 2017; 36:627–30.
11. Freitas
AC et al., Clin Infect Dis 2013; 56:1451–6.
12. Watts
DH, et al., Am J Obstet Gynecol 1998; 178:365–73.
13. Zahreddine
M et al., EClinicalMedicine 2020; 21:100334.
Luigi Raio
Mammographiescreening ab 40 Jahren?
Die Autoren berichten über den UK Age Trial, welcher zwischen 1990 und 1997 Frauen rekrutierte, um den Effekt des jährlichen Mammographiescreenings ab dem 40. Lebensjahr zu untersuchen. Es handelt sich um eine randomisierte, kontrollierte Studie, die an 23 Brustscreening-Einheiten in Grossbritannien stattfand. Insgesamt wurden 160 921 Frauen rekrutiert, davon wurden 53 883 in die Interventionsgruppe randomisiert (jährliche MG zwischen 40. und 48. Lebensjahr) und 106 953 in die Kontrollgruppe (keine MG bis 50. Lebensjahr). Ab dem 50. Lebensjahr erhielten die Frauen alle die in Grossbritannien übliche Einladung zum regulären Mammographiescreening. Der primäre Endpunkt dieser Studie war die brustkrebsassoziierte Mortalität während der Interventionsphase.
In der vorliegenden Analyse werden die Daten zum Langzeit-Follow-up dargestellt. Das mediane Follow-up lag bei 22.8 Jahren (IQR 21.8–24.0). Die Autoren beobachteten eine signifikante Reduktion der brustkrebsassoziierten Mortalität nach zehn Jahren Follow-up: 83 Brustkrebstodesfälle in der Screening-Gruppe vs. 219 Brustkrebstodesfälle in der Kontrollgruppe (relative rate [RR] 0.75 [95 % CI 0.58–0.97]; p = 0.029). Nach mehr als zehn Jahren Follow-up war die Reduktion der Todesfälle nicht mehr signifikant, in absoluten Zahlen jedoch weiterhin nachvollziehbar: 126 vs. 255 Todesfälle (RR 0.98 [0.79–1.22]; p =0.86) (Duffy et al., Lancet Oncol 2020; 21:1165–72).
Kommentar
Die jährliche Mammographie ab dem 40. Lebensjahr war in der hier publizierten Studie mit einer signifikanten Reduktion der brustkrebsassoziierten Mortalität während der Interventionsphase assoziiert (gegenüber einer Kontrollgruppe, die keine MG erhielt). Ab dem 50. Lebensjahr (ab dem sowohl die Interventions- als auch Kontrollgruppe das reguläre Screening erhielten) war die relative Reduktion nicht mehr so ausgeprägt, aber die absolute Reduktion an Todesfällen blieb konstant. Der Effekt an „Überdiagnosen“ in den ersten zehn Jahren schien nicht wesentlich erhöht zu sein, und die Autoren beobachteten auch keinen Schaden bezüglich einer erhöhten Strahlenexposition.
Cornelia Leo
Schlechter Outcome der Schwangerschaft und spätere Entwicklung von rheumatologischen Erkrankungen
Die Schwangerschaft als Belastungstest für das Leben war schon einige Male Thema in der FHA. Dabei wissen wir ja zur Genüge, dass speziell die hypertensiven Erkrankungen ein deutlich erhöhtes Risiko für kardiovaskuläre Erkrankungen später im Leben darstellen. So haben Frauen mit Zustand nach schwerer Präeklampsie ein signifikant höheres Risiko, eine Hypertonie zu entwickeln oder an einem Herzinfarkt oder Hirnschlag zu sterben als Frauen mit normalem Schwangerschaftsoutcome [1]. Wir wissen auch, dass vorbestehende Krankheiten, welche mit einer endothelialen Störung einhergehen, das Risiko für eine hypertensive Erkrankung in einer Schwangerschaft signifikant erhöhen. Zu nennen sind dabei vorbestehende Hypertonie oder renale Krankheiten, metabolische Störungen wie Adipositas oder Diabetes wie auch hämatologische und rheumatologische Erkrankungen wie v. a. ein systemischer Lupus erythematodes (SLE), ein Antiphospholipidsyndrom (APS) und andere Bindegewebserkrankungen. Vor allem das APS wird bei uns in der Präeklampsie-Nachsorgesprechstunde gesucht, insbesondere bei den frühen Präeklampsien <34 Wochen.
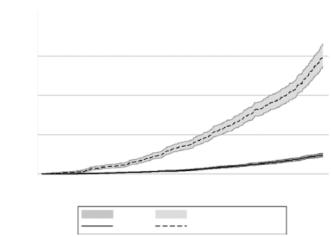
Nun, dass der ungünstige Ausgang der Schwangerschaft auch mit einem höheren Risiko für die spätere Entwicklung ebendieser Krankheiten aus dem rheumatologischen Formenkreis assoziiert sein kann, ist relativ neu [2]. In einer grösseren epidemiologischen Studie wurden Frauen mit „ungünstigem“ Schwangerschaftsoutcome mit solchen mit normalem Verlauf verglichen. Insgesamt wurden etwas mehr als 20 000 pathologische Schwangerschaften mit knapp 100 000 normalen verglichen (fünf Kontrollen pro Fall). Die mediane Beobachtungszeit lag bei 7.3 Jahren. Im Vergleich betrug das Risiko für die Entwicklung von rheumatologischen Krankheiten oder Autoantikörpern 3.2 (95 %CI 2.90–3.51) (Abb. 1). Am höchsten war das Risiko nach intrauterinem Tod (RR 5.82 [95 %CI 4.97–6.81]). Das Risiko für ein SLE oder eine andere Bindegewebserkrankung war am höchsten in den ersten fünf Jahren nach der Geburt, während Antiphospholipid-Ak oder ein APS nach fünf Jahren gehäuft diagnostiziert wurde (RR 5.64 [95 %CI 1.27–27.16; p = 0.02]).
Das sind sehr interessante Erkenntnisse, welche zeigen, dass neben der endothelialen Dysfunktion Autoimmunprozesse kausal mit der Entwicklung einer Präeklampsie assoziiert sein können. Es stellt sich hier die Frage, was ist Huhn und was das Ei!? In dieser Arbeit wurden Datenbanken und Diagnosecodes gekoppelt und Inzidenzen gesucht. Es ist nicht klar, ob diese Frauen zum Zeitpunkt der Geburt bereits Hinweise für autoimmune Probleme aufgewiesen haben oder nicht. Aus meiner Erfahrung der letzten 20 Jahre Nachsorge von PE-Fällen sind etwa 14 % der Frauen bereits 6–12 Wochen nach der Geburt positiv für aPL-Ak und einige Prozent dieser Frauen weisen „unspezifische“ Erhöhungen der antinukleären Antikörper auf. Ich bin eher der Meinung, dass eine saubere, postnatale Abklärung dieser Frauen viele solcher Probleme frühzeitig aufzudecken vermag, bevor die Frau mit Thrombosen, Hirnschlag, mit terminalen Nierenerkrankungen oder SLE-bedingten Folgeschäden den Internisten auffallen!
Literatur
1. Raio
L., FHA 2011; 4:23–8.
2. Kither
H. et al., BJOG 2020; 127:941–9.
Luigi Raio ■